A)L’hydrogène de l’urée.
Le dihydrogène est la forme moléculaire de l'élément hydrogène. Les molécules comportent deux atomes d'hydrogène, sa formule chimique est H2. Il est également appelé « molécule d'hydrogène » ou « gaz hydrogène » et, dans le langage courant, lorsqu'il n'y a pas d'ambiguïté avec l'élément chimique du même nom, il est très fréquemment désigné par « hydrogène ».
Il brûle dans l'air en produisant de l'eau, d'où son nom composé par le préfixe « hydro », du grec ὕδωρ (hudôr) signifiant « eau », et par le suffixe « gène », du grec γεννᾰν (gennen), « engendrer.
Il existe un grand nombre de moyen de produire du dihydrogène, l'hydrogène étant intégré à de nombreuses molécules chimiques (eau, urine, hydrocarbures, sucres, etc.)}
Actuellement seulement 1 % de la production d’hydrogène est utilisée comme vecteur énergétique, uniquement dans le cadre des applications spatiales.
Il est important de préciser que l'hydrogène produit actuellement n'est pas une source primaire d'énergie mais seulement un mode de stockage, un peu comme une batterie.
Afin d'être une énergie vraiment avantageuse en termes d'environnement, l'hydrogène doit pouvoir être produit à partir d'énergie renouvelable.
Nous allons étudier les molécules de dihydrogène dans l’urée.
Il brûle dans l'air en produisant de l'eau, d'où son nom composé par le préfixe « hydro », du grec ὕδωρ (hudôr) signifiant « eau », et par le suffixe « gène », du grec γεννᾰν (gennen), « engendrer.
Il existe un grand nombre de moyen de produire du dihydrogène, l'hydrogène étant intégré à de nombreuses molécules chimiques (eau, urine, hydrocarbures, sucres, etc.)}
Actuellement seulement 1 % de la production d’hydrogène est utilisée comme vecteur énergétique, uniquement dans le cadre des applications spatiales.
Il est important de préciser que l'hydrogène produit actuellement n'est pas une source primaire d'énergie mais seulement un mode de stockage, un peu comme une batterie.
Afin d'être une énergie vraiment avantageuse en termes d'environnement, l'hydrogène doit pouvoir être produit à partir d'énergie renouvelable.
Nous allons étudier les molécules de dihydrogène dans l’urée.
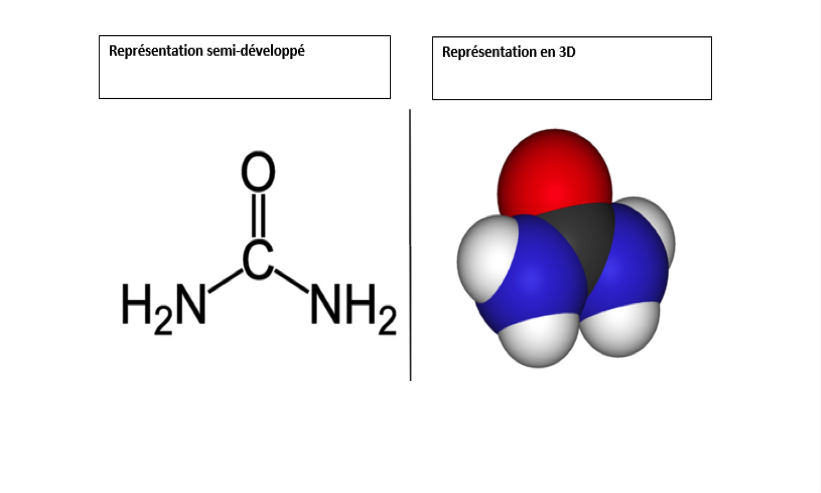
L'urée ou carbamide (DCI) est un composé organique de formule chimique CO(NH2)2. C'est aussi le nom de la famille des dérivés de l'urée de formule générale (R1,R2)N-CO-N(R3,R4).
L'urine contient environ 2% d'urée. Chaque molécule d'urée contient quatre atomes d'hydrogène, qui sont moins fortement fixés à l'urée que l'hydrogène ne l'est à l'eau. Par conséquent, séparer l'hydrogène de l'urée demande moins d'énergie que de l'eau et permet une production d'hydrogène plus efficace.

En 2002, l’idée de produire de l’électricité grâce à l’urine est venue à l'esprit de Gerardine Botte, chimiste à l'université de l'Ohio.
L'hydrogène n'existe pratiquement pas à l'état pur, il faut donc le produire avant de l'utiliser. On peut produire de l'hydrogène en grande quantité avec des hydrocarbures, mais ce n'est pas évident à stocker et à distribuer. L'autre possibilité est de séparer l'hydrogène et l'oxygène de l'eau pour introduire directement de l'hydrogène dans une pile à combustible... mais le processus de séparation de l'hydrogène de l'eau consomme autant d'énergie que l'hydrogène en produit ensuite.
L'idée de Botte est d'utiliser de l'urine à la place de l'eau
L'hydrogène n'existe pratiquement pas à l'état pur, il faut donc le produire avant de l'utiliser. On peut produire de l'hydrogène en grande quantité avec des hydrocarbures, mais ce n'est pas évident à stocker et à distribuer. L'autre possibilité est de séparer l'hydrogène et l'oxygène de l'eau pour introduire directement de l'hydrogène dans une pile à combustible... mais le processus de séparation de l'hydrogène de l'eau consomme autant d'énergie que l'hydrogène en produit ensuite.
L'idée de Botte est d'utiliser de l'urine à la place de l'eau
B) Technique pour l'Extraire
Définition : L'électrolyse est une méthode qui permet de réaliser des réactions chimiques grâce à une activation électrique. C'est le processus de conversion de l'énergie électrique en énergie chimique. Elle permet par ailleurs, dans l'industrie chimique, la séparation d'éléments ou la synthèse de composés chimiques. La matière à décomposer ou à transférer est dissoute dans un solvant approprié, ou fondue de sorte que ses ions constitutifs soient disponibles dans la solution. Une différence de potentiel électrique est appliquée entre deux électrodes immergées dans cette solution. La cathode est le siège d'une réduction (gain d’électrons) et, l'anode le siège d'une oxydation (perte d’électrons). Le potentiel de l'anode étant supérieur -ou égal dans une pile court circuitée- au potentiel de la cathode, on peut dire que l'anode est la borne positive et que la cathode est la borne négative. Notons que ces bornes sont inversées dans le cas d'une pile. Lors du passage d'un courant électrique continu, les électrodes attirent à elles les ions de charges opposées.
Le mécanisme d'électrolyse qui va briser la molécule utilise une nouvelle électrode peu coûteuse à base de nickel pour oxyder sélectivement et efficacement l'urée. De là, une tension de 0.37V est appliquée à travers la cellule pour briser la molécule, bien en deçà des 1,23V nécessaires pour décomposer l'eau.
Au cours du processus électrochimique, l'urée est absorbée sur la surface de l'électrode de nickel, où circule l'électron nécessaire pour casser la molécule. De l'hydrogène pur a été produit au niveau de la cathode, tandis que de l'azote et du dioxyde de carbone se formaient à l'anode.
NB : Gerardine Botte montre qu'avec de meilleures électrodes, on pourrait produire de l'hydrogène à partir d'urine pour moins d'un dollar par kilogramme. Cette technologie pourrait alors s'avérer utile dans les endroits de grandes quantités d'urine sont collectées.
Le mécanisme d'électrolyse qui va briser la molécule utilise une nouvelle électrode peu coûteuse à base de nickel pour oxyder sélectivement et efficacement l'urée. De là, une tension de 0.37V est appliquée à travers la cellule pour briser la molécule, bien en deçà des 1,23V nécessaires pour décomposer l'eau.
Au cours du processus électrochimique, l'urée est absorbée sur la surface de l'électrode de nickel, où circule l'électron nécessaire pour casser la molécule. De l'hydrogène pur a été produit au niveau de la cathode, tandis que de l'azote et du dioxyde de carbone se formaient à l'anode.
NB : Gerardine Botte montre qu'avec de meilleures électrodes, on pourrait produire de l'hydrogène à partir d'urine pour moins d'un dollar par kilogramme. Cette technologie pourrait alors s'avérer utile dans les endroits de grandes quantités d'urine sont collectées.
C)Produire de l'Electricité
Définition : Une pile à combustible est une pile dans laquelle la fabrication de l'électricité se fait grâce à l'oxydation(perte d’électrons) sur une électrode d'un combustible réducteur (réactif oxydé) couplée à la réduction(gain d’électrons) sur l'autre électrode d'un oxydant(réactif réduit).
La pile à hydrogène est une pile à combustible utilisant le dihydrogène et le dioxygène. Il s’agit d’une combustion électrochimique et contrôlée de dihydrogène et de dioxygène, avec production simultanée d’électricité, d’eau et de chaleur, selon la réaction chimique de fonctionnement de la pile :
2 H2 (g) + O2 (g) = 2 H2O (l)
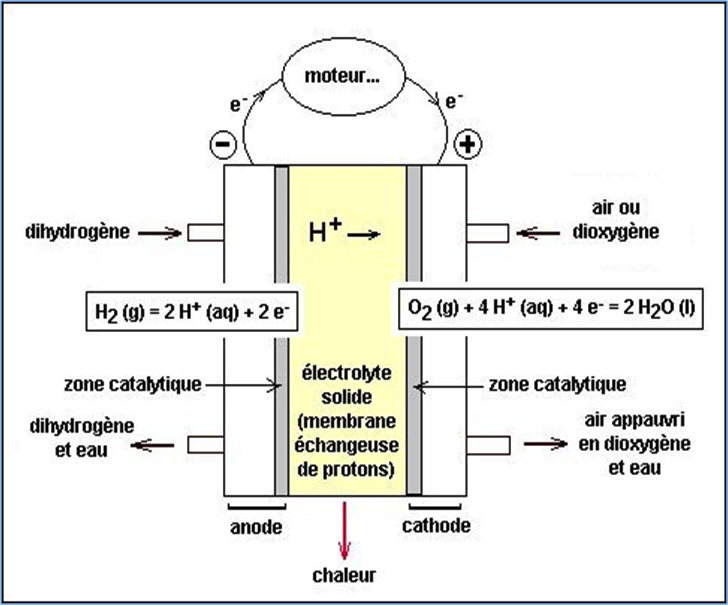
Pour mettre en œuvre cette réaction, on dispose de deux électrodes l’anode et la cathode séparées par un électrolyte (milieu bloquant le passage des électrons mais laissant circuler les ions). Cette réaction est déclenchée en utilisant un catalyseur, en général du platine.
L’hydrogène, provenant d’un réservoir, est dirigés vers l’anode pour y être dissocié selon la demi-équation électronique: H2 (g) = 2 H+ (aq) + 2 e-
Les ions H+, attirés par la cathode, passent au travers de l’électrolyte ; les électrons e-, attirés par l’anode, sont bloqués par l’électrolyte et récupérés dans un circuit interne.
L’oxygène, provenant de l’air, est dirigé vers la cathode. En y rencontrant les ions H+, il se combine avec eux et provoque la combustion de l’hydrogène, ce qui fournit de la chaleur et de l’eau. La demi-équation électronique : O2 (g) + 4 H+ (aq) + 4 e- = 2 H2O (l)
Lors de l’électrolyse de l’urine les réactions qui se produisent aux électrodes sont inverses de celles de la pile.
Schéma de principe d'une pile à électrolyte polymère solide
La pile à hydrogène est une pile à combustible utilisant le dihydrogène et le dioxygène. Il s’agit d’une combustion électrochimique et contrôlée de dihydrogène et de dioxygène, avec production simultanée d’électricité, d’eau et de chaleur, selon la réaction chimique de fonctionnement de la pile :
2 H2 (g) + O2 (g) = 2 H2O (l)
Pour mettre en œuvre cette réaction, on dispose de deux électrodes l’anode et la cathode séparées par un électrolyte (milieu bloquant le passage des électrons mais laissant circuler les ions). Cette réaction est déclenchée en utilisant un catalyseur, en général du platine.
L’hydrogène, provenant d’un réservoir, est dirigés vers l’anode pour y être dissocié selon la demi-équation électronique: H2 (g) = 2 H+ (aq) + 2 e-
Les ions H+, attirés par la cathode, passent au travers de l’électrolyte ; les électrons e-, attirés par l’anode, sont bloqués par l’électrolyte et récupérés dans un circuit interne.
L’oxygène, provenant de l’air, est dirigé vers la cathode. En y rencontrant les ions H+, il se combine avec eux et provoque la combustion de l’hydrogène, ce qui fournit de la chaleur et de l’eau. La demi-équation électronique : O2 (g) + 4 H+ (aq) + 4 e- = 2 H2O (l)
Lors de l’électrolyse de l’urine les réactions qui se produisent aux électrodes sont inverses de celles de la pile.
Schéma de principe d'une pile à électrolyte polymère solide
La pile à combustible peut intervenir dans une large gamme de températures, de 70°C à 1000°C.Selon la température retenue, la nature de l’électrolyte et les électrodes, les réactions chimiques intermédiaires mises en jeu varient mais le principe général reste le même.
En élevant la température, les réactions sont plus rapides, ce qui accroît le débit de la pile, mais les problèmes techniques spécifiques liés aux hautes températures limitent ces aspects.
Ci-contre : Pile à hydrogène développée par le CEA (Commissariat à l'Energie Atomique) ; puissance :
En élevant la température, les réactions sont plus rapides, ce qui accroît le débit de la pile, mais les problèmes techniques spécifiques liés aux hautes températures limitent ces aspects.
Ci-contre : Pile à hydrogène développée par le CEA (Commissariat à l'Energie Atomique) ; puissance :
Cette pile combustible ne rejettent que de l'eau, et dispose d'un rendement élevé car elle assure en une seule étape le passage de l'énergie chimique à l'énergie électrique.
Son intérêt majeur consiste à fournir de l’électricité sans être relié au réseau électrique et, surtout, à fournir cette énergie sans émission de dioxyde de carbone. Elle transforme directement en électricité l’énergie.
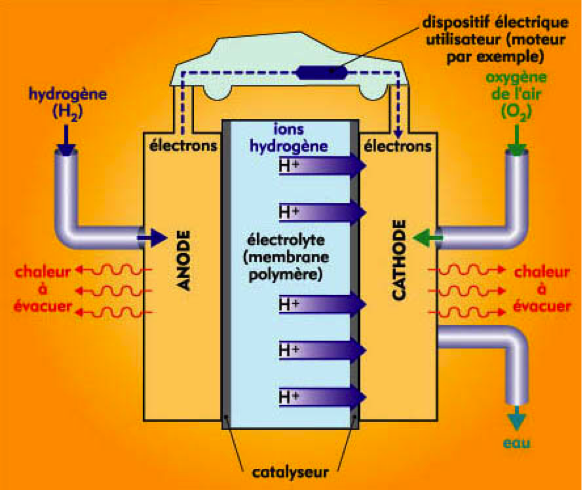
Exemple au niveau des automobiles :
Son intérêt majeur consiste à fournir de l’électricité sans être relié au réseau électrique et, surtout, à fournir cette énergie sans émission de dioxyde de carbone. Elle transforme directement en électricité l’énergie.
Exemple au niveau des automobiles :
Voici un slide show représentant la production de l’élèctricite à partir de l’hydrogène:
D) À quel stade de développement de cette technologie en est-on?
La start-up new yorkaise SiGNa Chemistry développe des piles à combustible fonctionnant avec de l’urine. L’armée américaine teste cette nouvelle technologie afin d’alléger l’équipement des soldats.
La société SiGNa Chemistry fabrique des mini-piles à combustible qui rechargent notamment les smartphones.
La start-up teste sa technologie avec l’armée américaine. Sur les champs de bataille, pour alimenter ces piles, il suffira d’une minuscule cartouche à hydrogène chimique et un peu d’urine. Lampes de poche, équipements informatiques, dispositifs de vision et de visées nocturnes pourront être rechargés en milieux hostiles.
Les piles à combustibles sont non toxiques, n’ont pas besoin d’être rechargées, et se manipulent en toute sécurité. L’ajout d’eau ou d’urine déclenche une réaction chimique qui génère instantanément de l’électricité.
Le PDG, Michael Lefenfeld, souligne qu’en adoptant cette technologie, les équipements des soldats seraient allégés de 11 kilos.
La diminution voire l’élimination des combustibles fossiles simplifie la logistique de guerre, réduit les coûts de maintenance et élimine le risque d’attaque contre les convois de carburant. Le choix de l’énergie verte est donc bien tactique.
Cette nouvelle technologie a été présentée aux Etats-Unis au mois de janvier, au Consumer Electronics Show de Las Vegas, sous la forme d’un chargeur de smartphone fonctionnant avec une pile à combustible.
Les cartouches ont une durée de conservation illimitée et peuvent être expédiées et stockées pendant de longues périodes sans aucun risque. Cette spécificité résulte d’une poudre de sodium inventée par SiGNa Chemistry. La poudre libère de l’hydrogène lorsqu’elle réagit à l’eau ou à l’urine tout en étant parfaitement stable.
La start-up new-yorkaise travaille actuellement avec ses partenaires pour fabriquer des produits de plus grande capacité afin de recharger des IPad ou des ordinateurs portables.
La société SiGNa Chemistry fabrique des mini-piles à combustible qui rechargent notamment les smartphones.
La start-up teste sa technologie avec l’armée américaine. Sur les champs de bataille, pour alimenter ces piles, il suffira d’une minuscule cartouche à hydrogène chimique et un peu d’urine. Lampes de poche, équipements informatiques, dispositifs de vision et de visées nocturnes pourront être rechargés en milieux hostiles.
Les piles à combustibles sont non toxiques, n’ont pas besoin d’être rechargées, et se manipulent en toute sécurité. L’ajout d’eau ou d’urine déclenche une réaction chimique qui génère instantanément de l’électricité.
Le PDG, Michael Lefenfeld, souligne qu’en adoptant cette technologie, les équipements des soldats seraient allégés de 11 kilos.
La diminution voire l’élimination des combustibles fossiles simplifie la logistique de guerre, réduit les coûts de maintenance et élimine le risque d’attaque contre les convois de carburant. Le choix de l’énergie verte est donc bien tactique.
Cette nouvelle technologie a été présentée aux Etats-Unis au mois de janvier, au Consumer Electronics Show de Las Vegas, sous la forme d’un chargeur de smartphone fonctionnant avec une pile à combustible.
Les cartouches ont une durée de conservation illimitée et peuvent être expédiées et stockées pendant de longues périodes sans aucun risque. Cette spécificité résulte d’une poudre de sodium inventée par SiGNa Chemistry. La poudre libère de l’hydrogène lorsqu’elle réagit à l’eau ou à l’urine tout en étant parfaitement stable.
La start-up new-yorkaise travaille actuellement avec ses partenaires pour fabriquer des produits de plus grande capacité afin de recharger des IPad ou des ordinateurs portables.